2024-04-08 阅读量:89
青光眼是一种神经退行性疾病,也是世界范围内不可逆失明的主要原因,其特征是进行性视神经变性和视网膜神经节细胞(RGCs)丢失。由于RGCs凋亡通常出现在病程的晚期,所以尽管RGC细胞凋亡对疾病发展至关重要,目前针对青光眼的研究仍主要倾向于淡化RGCs死亡,并更加注重研究早期轴突损伤。RGCs高度极化并具有长轴突,轴突运输对于视觉通路中维持适当的神经元功能尤为重要。轴突转运缺陷已被证明是青光眼和其他神经退行性疾病轴突变性最早期的关键病理生理变化。眼压升高(IOP)是青光眼最重要的风险因素之一。既往研究显示,出现IOP的眼中,视神经乳头(ONH)两端的压差增加,压迫视神经,从而阻碍顺行和逆行轴突运输。然而,这一过程的关键特征和早期干预的意义仍有待进一步探讨。
CD82是四次跨膜蛋白超家族中的膜糖蛋白。四次跨膜蛋白家族在进化上是保守的,调节免疫系统、肿瘤和细胞增殖。几种四次跨膜蛋白在神经元信号传导和视网膜变性中也起着关键作用。CD82广泛表达在人体组织中,并是众所周知的肿瘤抑制蛋白。然而,CD82对神经元系统(NS),特别是视网膜中NS的影响,尚不清楚。
哺乳动物雷帕霉素靶蛋白(mTOR)通路的失调与神经退行性疾病有关,如阿尔茨海默病、帕金森病和青光眼。数项研究表明,mTOR途径在维持RGCs的适当结构和功能方面发挥作用,mTOR组成部分在视网膜内层表达,mTORC1主要定位于RGCs及其轴突,因此直接参与RGCs轴突功能的调节。此外,mTOR途径的蛋白也可与四次跨膜蛋白超家族成员发生相互作用,如TSPAN8、CD9。
近期,华中科技大学同济医学院附属同济医院张虹主任医师团队在Cell Death & Disease期刊在线发表名为“CD82 protects against glaucomatous axonal transport deficits via mTORC1 activation in mice”研究论文,在本研究中,作者借助急性高眼压(AOHT)小鼠模型研究了CD82在轴突运输缺陷及轴突变性中的作用。研究人员发现急性IOP后CD82表达瞬态下调,同时出现轴突运输缺陷。利用AAV2/9载体在小鼠视网膜中过表达CD82改善了视神经轴突运输并减轻了随后的轴突变性。此外,小鼠视神经挤压(ONC)模型中CD82的过表达刺激了视神经再生并恢复视力。进一步探究显示CD82通过激活mTOR途径,从而发挥神经保护作用。综上所述,本文研究结果揭示了一种新的神经保护机制,并为青光眼的治疗提供了一个潜在治疗靶点。

1、小鼠急性高眼压模型早期阶段CD82在视网膜、ONH和ON中表达下调
研究人员首先在小鼠中构建AOHT模型,并于造模后不同时间点检测(无髓)视神经乳头ONH、(后有髓)视神经ON、视网膜中CD82蛋白表达水平,免疫染色和Western blot结果一致地显示造模后8 h CD82蛋白表达开始下降、第2天(Day 2)到达最低水平,而Day 7表达水平部分恢复。进一步研究CD82在眼中的细胞定位,结果表明CD82主要与RGCs标志物Tuj1共定位。提示CD82主要在RGCs及其轴突中发挥作用。
图1. 急性眼压升高后早期阶段视网膜、ONH和ON中CD82表达下调
2、AOHT后CD82的过表达发挥对轴突运输缺陷的保护作用
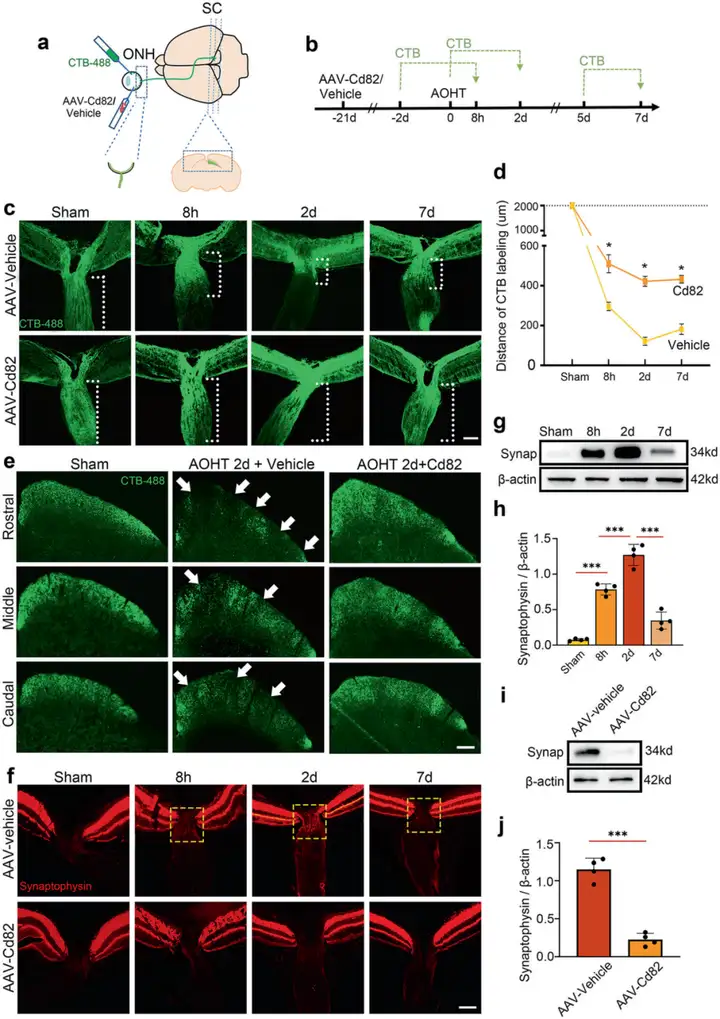
研究人员利用玻璃体腔注射重组腺相关病毒rAAV2/9-Cd82-mCherry成功在视网膜和ON中过表达CD82,接下来,作者重点关注ONH(青光眼视神经病变的关键位点)与上丘SC(啮齿类动物脑中RGCs的主要投射靶点)的损伤,首先,利用眼内注射霍乱毒素β亚基(CTB)可视化视神经顺行运输功能,CTB通过主动摄取和运输标记整个视网膜投射,ONH切片显示假手术组CTB沿整个轴突长度(>2000 μm)均匀分布。但诱导AOHT后,CTB不能远距离运输,Day 2遇到严重障碍(<200 μm),Day 7略有恢复。值得注意的是CD82过表达逆转了这种障碍并在Day 2将CTB标记距离保持在400 μm以上。此外,在连续序列切片头端、中间和尾部三层中均观察到SC中CTB信号强度,并显示到达脑的运输中断。对照组中SC具有完整的CTB分布,AOHT后CTB信号分布不均匀,在所有三层中都有大量缺陷。而注射AAV-Cd82的AOHT小鼠的SC表现出较低的CTB标记损失。随后,作者通过突触素的免疫荧光染色评估内源物质运输,突触素是RGCs合成的囊泡转运标志物,并沿着ON顺行转运。在正常情况下,ONH中没有蛋白沉积。然而,AOHT造模后8 h内,突触素蛋白开始在ONH沉积,并在Day 2达到峰值(蛋白沉积量最大)。而在注射AAV-Cd82组,这种蛋白沉积显著减少。ONH中提取蛋白的Western blot实验结果也显示AOHT造模后突触素蛋白表达明显增加,并证实CD82的保护作用。
图2. CD82过表达改善急性高眼压后轴突运输缺陷
3、CD82过表达减轻视神经由AOHT诱导的轴突变性
由轴突运输缺陷随之而来的病理学表现是视神经轴突变性,视神经轴突变性更严重,更难逆转。于是,研究人员检测AOHT后视神经轴突变性变化,神经纤维层中Tuj1的免疫荧光染色显示神经节细胞的轴突。结果显示AOHT组出现轴突丢失,表现为免疫荧光更弱和轴突分布更稀疏。而CD82过表达后,轴突分布几乎完好无损。但RGCs胞体在这一阶段没有明显丢失,表明轴突变性是一种早于RGCs死亡的早期病理变化。早期轴突丢失和后期RGCs胞体死亡之间存在的时间滞后与先前的研究结果一致。
4、CD82过表达促进视神经挤压(ONC)模型中轴突再生、RGCs存活和视觉功能
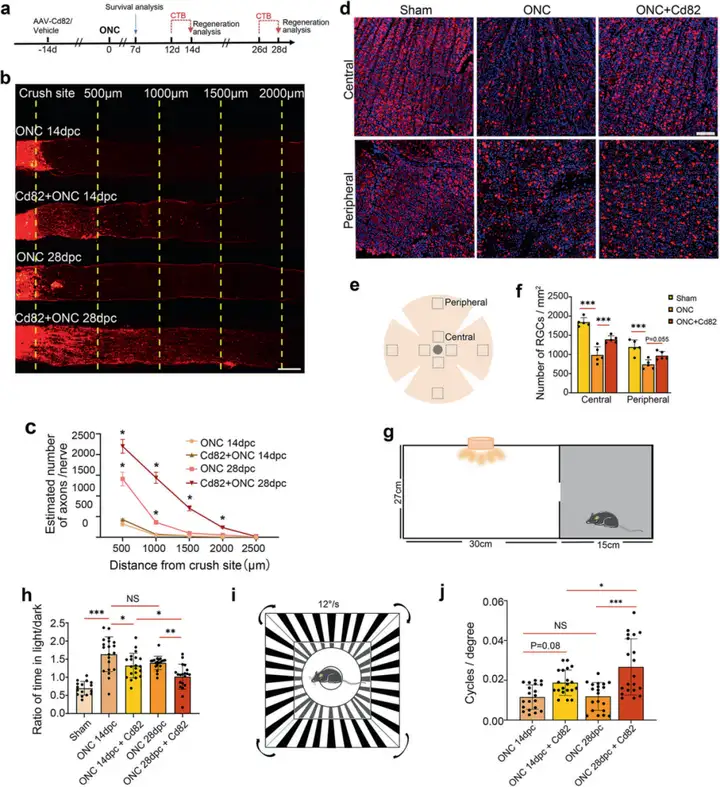
目前,逆转视神经损伤、恢复晚期青光眼(已出现大量轴突损伤和RGCs丢失)视力的方法非常有限。研究人员构建损伤更显著的模型,即视神经挤压(ONC),通过直接中断轴浆运输导致明显的神经元丢失和快速的轴突损伤(与晚期青光眼损伤程度相当),并在该模型中诱导CD82的过表达。利用CTB追踪ONC后轴突再生,结果显示Cd82+ONC组,再生和生长的RGCs轴突纤维在Day 14延伸超过挤压部位1 mm(1000 μm),并在Day 28延伸到2 mm(2000 μm),而无论恢复时间如何,ONC组都没有可见的轴突再生。此外,ONC后7天,在视网膜铺片中通过RBPMS(具有多重剪接的RNA结合蛋白,RGCs的优秀标记物)免疫荧光染色评估RGCs存活率。结果显示CD82过表达后RGCs存活率的提高在中央视网膜中是显著的,而在外围区域则没有显而易见。随后,通过小鼠视觉功能实验测试RGCs的功能,进行明暗室穿梭实验测量双侧ONC小鼠的光感(LP),结果显示ONC小鼠在暗室内的停留时间缩短,反映了视力的丧失。此外,ONC小鼠在光/暗室内停留时间比例增加,而CD82过表达使得ONC小鼠光/暗室内停留时间比例明显下降,表明CD82处理后LP的恢复。研究人员对小鼠进行高对比度视觉刺激以测量视动反应从而反映视力。双侧ONC后Day 28,相比于仅ONC小鼠,注射AAV-Cd82的ONC小鼠空间频率阈值更高(捕捉到更高旋转速度的图案),证明其视力的提高。综上所述,CD82过表达后小鼠视觉依赖行为得以恢复,证明了其改善视神经损伤后视觉功能的能力。
图3. CD82过表达促进ONC模型中轴突再生、RGCs存活和视觉功能
5、CD82过表达通过mTORC1依赖性机制发挥对轴突运输缺陷的改善作用
mTOR信号通路对调节神经元功能至关重要,随后,作者推测mTOR通路是否是CD82介导的保护作用所必需的。蛋白免疫印迹结果说明H2O2处理(100 μM,模拟视网膜变性的细胞损伤)的人胚肾细胞(HEK-293T)中磷酸化pS6K(p70 S6 Kinase:促分裂原激活的Ser/Thr蛋白激酶,mTORC1下游已知效应器,p-pS6K)表达下调,但在CD82过表达后恢复。此外,CD82诱导的p-pS6K表达增加被雷帕霉素(rapamycin)阻断,而rapamycin是mTOR的强效和特异性抑制剂,从而证实了mTORC1途径参与CD82的下游。这些调节关系也在视网膜组织中得到证明。AOHT组视网膜铺片中p-pS6K(红色)和RGCs标记物Tuj1(绿色)的免疫荧光染色共定位减少,而CD82过表达阻碍了这种减少,但rapamycin处理减少了CD82的信号激活作用(p-pS6K与Tuj1的染色共定位依然减少)。
接下来,进一步验证mTORC1活性在调节CD82提高的轴突运输功能中的作用,研究人员在体内实验中连续28天每两天添加一次雷帕霉素处理以阻断mTOR活性,结果显示在这种情况下,CD82的过表达未能缓解AOHT诱导的轴突运输缺陷,表现为突触素蛋白在ONH的沉积和CTB从眼睛到SC的运输损伤。考虑到药理学抑制剂雷帕霉素由于系统给药和低组织特异性而产生的混杂效应,作者使用条件性敲除小鼠来靶向RGCs,通过将AAV-hSyn-Cre注射到Rptorfl/fl小鼠玻璃体来删除Raptor,而由于Raptor是mTORC1的专一性功能组分,从而验证了RGCs中mTORC1通路的特异性作用。结果首先证实Rptorfl/fl小鼠注射Cre酶眼睛中mTORC1通路的失活。而轴突运输的评估与之前的结果一致,表明RGCs中mTORC1活性的抑制阻断了CD82的保护作用。
图4. CD82过表达通过mTORC1依赖性机制来改善轴突转运缺陷
结论
综上,本研究揭示了CD82在AOHT后通过mTORC1激活发挥保护作用,有效缓解轴突运输缺陷和随后的轴突变性。本研究首次探究了CD82在眼科神经退行性疾病中的作用,有助于填补这方面空白,获得了对四次跨膜蛋白更深入的了解,并为视神经保护提供了潜在的神经保护策略。
示意图:高眼压状态下CD82神经保护作用
华中科技大学同济医学院附属同济医院眼科教授张虹、助理研究员赵寅为本文共同通讯作者,叶萌(现为同济医院眼科医师)、黄静秋(现为中南医院眼科副研究员)为共同第一作者。该研究得到国家自然科学基金项目(Nos.31800868、Nos.81770921、Nos.82070965)等资助。
本文使用的病毒产品均来自枢密科技,列表如下:


了解产品及服务
请扫码或添加客服微信:BrainVTA2020

市场:027-65023363 行政/人事:027-62439686 邮箱:marketing@brainvta.com
销售总监:张经理 18995532642 华东区:陈经理 18013970337 华南区:王经理 13100653525 华中/西区:杨经理 18186518905 华北区:张经理 18893721749
地址:中国武汉东湖高新区光谷七路128号中科开物产业园1号楼
Copyright © 武汉枢密脑科学技术有限公司. All RIGHTS RESERVED.
鄂ICP备2021009124号 DIGITAL BY VTHINK